VÍA DE ADMINISTRACIÓN DE FÁRMACOS
RESUMEN:
Las vías de administración de fármacos son las rutas de entrada del medicamento al organismo, la cual influye en la latencia, intensidad y duración del efecto, por esta razón es de suma importancia conocer sus ventajas y desventajas además de cual de las vías de administración de fármacos se utiliza en una situación particular.
Vías de Administración de Fármacos-Definición
Ruta de entrada o los medios por los cuales los fármacos son introducidos al organismo para producir sus efectos
Parámetros afectados según la vía de administración de fármacos:
- rapidez de acción de los fármacos
- eficacia del fármaco
- efectos adversos de los fármacos
Vías de Administración de Fármacos
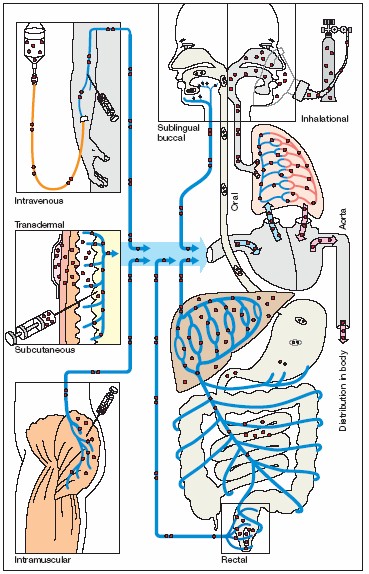
Enterales:
Los fármacos son introducidos al organismo por los orificios naturales del cuerpo.
Referente o relacionada al intestino o al tracto gastrointestinal.
- ORAL
- SUBLINGUAL
- RECTAL
Parenterales:
Los fármacos para ser introducidos al organismo, requiere la utilización de una aguja hueca hipodérmica, se crea un orificio no natural en el cuerpo.
Diferente o paralelo al intestino o al tracto gastrointestinal.
Intramuscular, Intraperitoneal
Subcutánea, Intraarticular
Intravascular, Intrapleural
Intravenosa Intraosea
Intraarterial Intratecal
Intracardiaca Intralinfática
Tópica:
Los medicamentos son aplicados a piel o mucosas para un efecto local.
Ejemplo de vías tópicas:
Auditiva Conjuntiva
Nasal Colon
Vaginal Uretra
Piel Vejiga
Transdérmica: los medicamentos son aplicados sobre la piel para un efecto sistémico.
Vías de Administración de Fármacos-ORAL
Ventajas: cómoda, sencilla, conveniente, común, económica, inocua, segura, permite la autoadministración
Desventajas:
irritación, absorción irregular, pH estomacal, presencia de alimentos, destrucción enzimática, efecto de primer paso, destrucción por bacterias, falta de colaboración del paciente
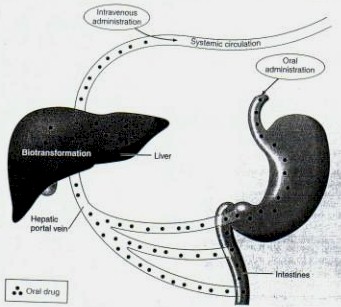
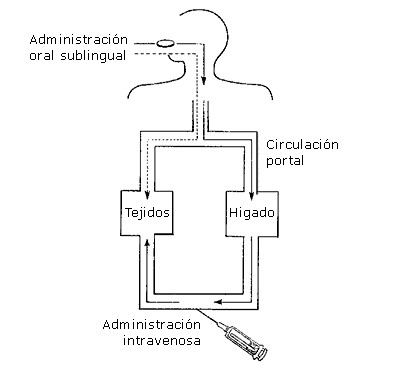
Vías de Administración de Fármacos-Sublingual
Ventajas: evita efecto de primer paso hepático, absorción rápida, efecto rápido, epitelio delgado, gran irrigación
Desventajas: área de absorción pequeña, no todos los medicamentos se pueden administrar por esta vía
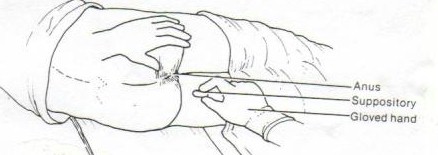
Vías de Administración de Fármacos-Rectal
Ventajas:útil en pacientes que no pueden deglutir, en vómitos intensos, pacientes inconscientes,
Desventajas: irritación, incómodo, absorción irregular e incompleta (heces, bacterias), puede sufrir efecto de primer paso hepático
Vías de Administración de Fármacos
Desventajas: irritación, incómodo, absorción irregular e incompleta (heces, bacterias), puede sufrir efecto de primer paso hepático
Vías de Administración de Fármacos
########
El 72% de los medicamentos autorizados en 2010 por la Agencia Española de Medicamentos y Productos Sanitarios fueron genéricos
- Según recoge la memoria de actividades del año 2010.
- En total, el año pasado se autorizaron 1.393 medicamentos de uso humano y 157 medicamentos de uso veterinario
- En materia de productos sanitarios se otorgó el marcado CE de conformidad a 192 productos, y también se autorizaron 114 nuevos productos de higiene personal
- El Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano recibió en 2010 más de 14.000 notificaciones de sospechas de reacción adversa
- En el ámbito de medicamentos ilegales y falsificados, la AEMPS llevó a cabo 105 actuaciones en colaboración con las Fuerzas y Cuerpos de Seguridad del Estado y, además, investigó 88 páginas web que vendían de forma ilegal medicamentos por Internet
- La AEMPS es un organismo líder en el desarrollo de procedimientos electrónicos para la resolución de trámites por vía telemática
25 de abril de 2011. La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) autorizó en 2010 la comercialización de 1.393 medicamentos, lo que supuso un 19% más que en 2009. De todos ellos, el 72% fueron medicamentos genéricos. Éste es uno de los principales datos extraídos de la memoria anual de actividad de la Agencia, que acaba de publicarse en su página web (http://www.aemps.es/).
La AEMPS es el organismo autónomo del Ministerio de Sanidad, Política Social e Igualdad responsable de garantizar a la sociedad la calidad, seguridad, eficacia y correcta información de los más de 13.000 medicamentos de uso humano autorizados y 3.000 medicamentos veterinarios, así como de los productos sanitarios, desde su investigación hasta su utilización. Todo ello en interés de la protección y promoción de la salud de las personas, de la sanidad animal y el medio ambiente.
La Agencia española es una de las más destacadas a nivel europeo, ya que ocupa el sexto lugar como ponente en los procedimientos de tipo centralizado para medicamentos de uso humano en el seno de la Agencia Europea de Medicamentos (EMA) y el cuarto lugar como Estado Miembro de Referencia en los procedimientos europeos de autorización de Reconocimiento Mutuo y Descentralizado de medicamentos veterinarios. Además, es una de las primeras Agencias en número de Inspecciones Internacionales de Normas de Buena Práctica Clínica, con 17 inspecciones durante el año 2010.
FUNCIONES
Entre su amplio abanico de actividades, se encuentran:
· La evaluación y autorización de medicamentos de uso humano y veterinario.
· El seguimiento de la seguridad de los medicamentos comercializados y el control de su calidad.
· La autorización e inspección de los laboratorios farmacéuticos.
· La supervisión del suministro y el abastecimiento de los medicamentos.
· La autorización de ensayos clínicos.
· La lucha contra los medicamentos y productos sanitarios ilegales y falsificados.
· La certificación, control y vigilancia de los productos sanitarios.
· El seguimiento de la seguridad de los cosméticos y los productos de higiene personal.
· La información de todo lo que tenga que ver con estos aspectos a los ciudadanos y profesionales sanitarios.
· La elaboración de la normativa que facilite el cumplimiento de sus funciones.
En 2010, la AEMPS ha desarrollado una labor intensa para que los ciudadanos dispongan de medicamentos, productos sanitarios, cosméticos y medicamentos veterinarios con todas las garantías exigibles.
En este sentido, además de la autorización decomercialización de 1.393 medicamentos de uso humano, de los cuales un 72% fueron medicamentos genéricos, se autorizaron 157 medicamentos de uso veterinario. A estas cifras hay que sumar las más de 21.000 solicitudes de variaciones de medicamentos ya autorizados.
PRODUCTOS SANITARIOS Y COSMÉTICOS
En el ámbito de los productos sanitarios, la AEMPS otorgó el marcado CE de conformidad europeo a 192 productos y prorrogó los certificados CE a otros 1.101 productos. Asimismo, llevó a cabo 104 auditorías de calidad a los fabricantes.
En cosméticos y productos de higiene personal, se autorizaron 114 productos de higiene y 346 modificaciones de productos ya autorizados. Además, se registraron 29.407 Informaciones a Efectos de Tratamiento Médico (IETMs) de cosméticos, lo que supuso 2.223 más que durante el año anterior. Esto refleja un aumento de comercialización de nuevos productos.
VIGILANCIA DE LA SEGURIDAD
Por lo que respecta a la vigilancia de la seguridad de todos los productos regulados por la AEMPS, hay que señalar que el Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano recibió en 2010 más de 14.000 notificaciones de sospecha de reacción adversa (en 2009 se notificaron más de 15.000). En el caso de los medicamentos veterinarios, las notificaciones de sospecha de efectos adversos fueron de 910 en 2010.
En productos sanitarios, la AEMPS recibe las notificaciones de incidentes adversos y de acciones correctivas de seguridad realizadas por los fabricantes y gestiona el Sistema de Vigilancia de Productos Sanitarios transmitiendo las alertas a las Comunidades Autónomas. Esta actividad registró un incremento significativo con respecto a añosanteriores con 2.354 notificaciones recibidas durante el año 2010 (460 más que en el año 2009) y 547 alertas transmitidas (123 más que en el año 2009).
En cosméticos se investigaron 18 efectos adversos y se transmitieron a las Comunidades Autónomas 127 alertas europeas.
La continua evaluación de estas señales de alarma, junto con la evidencia científica disponible, permite que la Agencia lleve a cabo diferentes acciones para proteger la salud de los ciudadanos; desde acciones informativas hasta la actualización de las fichas técnicas y prospectos, pasando por la retirada del mercado o suspensión de un medicamento si fuera necesario.
CONTROL DEL MERCADO Y MEDICAMENTOS ILEGALES
La AEMPS, en colaboración con las CCAA, desarrolla un programa de control de medicamentos en el mercado para controlar la calidad de los medicamentos autorizados en la cadena de distribución. La inclusión de medicamentos en este programa se realiza según los posibles riesgos. En este sentido, en 2010 se incluyeron en este programa 114 medicamentos. Además, el pasado año se investigaron 187 denuncias por defectos de calidad.
En el caso de medicamentos ilegales y falsificados, cabe destacar que en 2010 se registró una tendencia al alza en este tipo de intervenciones. Destaca el importante incremento en el número de muestras remitidas a los laboratorios de la Agencia por parte de los juzgados y Cuerpos y Fuerzas de Seguridad del Estado, que en 2010 llegó a la cifra de 2.041 (casi mil más que en 2009).
En el caso de investigaciones de páginas web que vendían de forma ilegal medicamentos por Internet, se realizaron 88 actuaciones (7 más que en 2009).
APOYO A LA INVESTIGACIÓN
La memoria de la AEMPS destaca también la labor importante que desempeña el organismo en materia de apoyo a la investigación clínica y en la autorización de ensayos clínicos. En materia de apoyo a la investigación, la Agencia cuenta con la Oficina de Apoyo a la Investigación Clínica Independiente, que ofrece asesoramiento a investigadores y promotores no comerciales, hasta el punto de que en 2010 se recibieron 537 consultas.
En cuanto a los ensayos clínicos, la Agencia autorizó el año pasado 643 ensayos clínicos y 133 productos en fase de investigación con medicamentos de uso humano, así como 23 ensayos clínicos y 9 productos en fase de investigación con medicamentos veterinarios. Además, se autorizaron 23 investigaciones clínicas con productos sanitarios.
Por último, hay que resaltar el liderazgo de la Agencia en materia de administración electrónica, ya que en la actualidad dispone de un total de 66 procedimientos electrónico mediante los cuales en 2010 se resolvieron más de 60.000 trámites por vía telemática.
La ministra Leire Pajín da a conocer los detalles de la primera cadena de trasplante renal de vivo con donante “buen samaritano".
########
La ministra Leire Pajín da a conocer los detalles de la primera cadena de trasplante renal de vivo con donante “buen samaritano".
- España culmina con éxito la primera cadena de donación entre vivos, realiza el pasado 6 de abril
- Seis personas han protagonizado el trasplante en cadena: un donante ‘buen samaritano’, dos parejas (dos donantes y dos receptores) y un receptor seleccionado de la lista de espera de donante fallecido, bajo riguroso criterio clínico.
- Leire Pajín: “Toda la sociedad española y todo el sistema sanitario público pueden sentirse orgullosos”
- Donantes y receptores han recibido el alta hospitalaria y se encuentran bien. Han sido intervenidos en la Fundación Puigvert de Barcelona y en el Hospital Virgen de las Nieves de Granada
- El trasplante en cadena permite incrementar el número de pacientes que se benefician de la donación renal de vivo, al combinar la figura del ‘buen samaritano’ con el trasplante renal cruzado entre parejas
- En este programa participan los 13 hospitales españoles actualmente acreditados para realizar trasplante renal cruzado
28 de abril de 2011. España ha realizado con éxito la primera cadena de trasplante renal de vivo con un ‘buen samaritano’. La cadena ha sido protagonizada por seis personas, que ya han recibido el alta y evolucionan favorablemente.
La ministra de Sanidad, Política Social e Igualdad, Leire Pajín, ha dado a conocer esta mañana los detalles de esta primera cadena de donación entre vivos en nuestro país. Ha estado acompañada por el director de la Organización Nacional de Trasplantes (ONT), Rafael Matesanz; y por los nefrólogos Luis Guirado (Fundación Puigvert de Barcelona) y Antonio Osuna (Hospital Virgen de las Nieves de Granada).
En su intervención, la ministra ha destacado que “hoy es un día en el que toda la sociedad española y todo el sistema sanitario público español pueden sentirse orgullosos”. En concreto, explicó que “toda donación es un acto altruista, pero el buen samaritano es el donante altruista por excelencia ya que se trata de una persona que dona un riñón a alguien que no conoce”.
Leire Pajín también señaló que “la generosidad de los ciudadanos y ciudadanas españoles es uno de los pilares fundamentales del liderazgo mundial de nuestro país en materia de donación y trasplantes”
Esta nueva modalidad del trasplante renal de vivo, combina el trasplante renal cruzado entre dos o más parejas que no se conocen entre sí, con la figura de un donante altruista que quiere donar su riñón a un desconocido.
Se trata de un donante altruista (también llamado ‘buen samaritano’, que dona un riñón a un desconocido), dos parejas (donante y receptor) incluidas en el registro de trasplante renal cruzado y un paciente con insuficiencia renal, procedente de la lista de espera de riñón de donante fallecido. Los seis fueron intervenidos el pasado 6 de abril en el Hospital Virgen de las Nieves de Granada y en la Fundación Puigvert de Barcelona.
La cadena se inicia con la donación renal del buen samaritano al receptor de una pareja. A su vez, el donante de esta pareja dona su riñón al receptor de una segunda y así sucesivamente hasta agotar todas las posibilidades de intercambio. El donante de la última pareja, por su parte, dona su riñón a un receptor de la lista de espera de fallecido, al que tampoco conoce, y que ha sido seleccionado bajo riguroso criterio clínico
El trasplante en cadena requiere una total colaboración entre la ONT, los coordinadores autonómicos de trasplantes, los hospitalarios y los profesionales de los equipos de trasplante que participan de este operativo. En esta primera ocasión han intervenido, además de los expertos de la ONT, la Coordinación Autonómica de Trasplantes de Cataluña, y la de Andalucía, así como un importante número de profesionales del hospital barcelonés y del granadino.
DONANTE ALTRUISTA
Aunque toda donación es por definición voluntaria, altruista y desinteresada, los expertos han decidido denominar ‘donante altruista’ (o ‘buen samaritano’) a aquella persona que dona un órgano a otra desconocida que necesita un trasplante. Se trata de una modalidad de donación de órganos, muy extendida en países como Holanda o Estados Unidos, pero que en nuestro país hasta ahora no se había desarrollado.
Dentro del programa para fomentar el trasplante renal de donante vivo, la Comisión de Trasplantes del Consejo Interterritorial del Sistema Nacional de Salud (donde están representadas la ONT y las Comunidades Autónomas) aprobó en 2010 incorporar la figura del ‘donante altruista’ o ‘buen samaritano’ a la donación renal de vivo en España.
La respuesta de los ciudadanos españoles no se ha hecho esperar. Desde que la ONT anunció su intención de desarrollar esta nueva forma de donación, un total de 35 personas han mostrado su disposición a convertirse en ‘donantes altruistas’. La mayor parte de ellos proceden de Andalucía, Madrid y Cataluña, aunque también se han registrado voluntarios de Aragón, Canarias, Castilla-León, Castilla-La Mancha, Navarra, Comunidad Valenciana y País Vasco.
De todos ellos, 1 ha finalizado ya la evaluación favorablemente, lo que ha permitido realizar este primer trasplante en cadena.
La puesta en marcha del trasplante en cadena también ha sido posible gracias al incremento progresivo del número de procedimientos y de hospitales que realizan trasplante renal de donante vivo, que alcanzaron en 2010 la cifra más alta de nuestra historia, con 240 trasplantes renales de donante vivo (que suponen un 11% de la actividad total de trasplante renal).
PROTOCOLO DEL TRASPLANTE EN CADENA
El estudio de los posibles candidatos a buen samaritano ha requerido tiempo. Para ello, la ONT, en colaboración con el comité de expertos del trasplante renal cruzado, ha desarrollado un protocolo de ‘donación altruista’ que incluye una evaluación completa del posible donante, tanto desde el punto de vista psicosocial, psiquiátrico y físico, con especial hincapié en sus motivaciones. Todos ellos son requisitos similares a los del procedimiento ya diseñado para el trasplante renal cruzado.
El protocolo se complementa con una evaluación rigurosa por parte del comité de ética del hospital donde se va a realizar el trasplante; la documentación a presentar ante el juez, que se ha consensuado con el poder judicial, y los pasos a seguir desde la solicitud del buen samaritano hasta finalizar el trasplante.
REQUISITOS
El trasplante renal de donante vivo está regulado en España por la Ley de trasplantes 30/1979, aplicada mediante el Real Decreto 2070/1999. La legislación española permite la donación en vida de un órgano, siempre y cuando esta donación sea compatible con la vida y la función del órgano o parte de él quede compensada por el organismo. Son condiciones que se dan en la donación renal de vivo. Y aunque no hace referencia a la figura del ‘buen samaritano’, nuestra ley permite la donación entre personas no relacionadas.
Al igual que sucede en la donación entre familiares, es imprescindible que el ‘donante altruista’ o ‘buen samaritano’ otorgue su consentimiento de forma expresa, libre y desinteresada. También debe ser mayor de edad, estar en plenas facultades y en perfecto estado de salud física y psíquica. Para ello será evaluado por diferentes profesionales sanitarios. El comité de ética del centro trasplantador, debe emitir además un informe favorable a la donación.
Posteriormente el donante declarará ante un juez del registro civil su voluntad de donar un riñón sin que medie condicionante alguno, en presencia del médico que va a efectuar la extracción, el coordinador hospitalario de trasplantes y el médico que ha certificado su estado de salud.
Como paciente, los únicos requisitos que se exigen es padecer una enfermedad renal que precise un trasplante y tener una pareja o un familiar donante no compatible.
Los hospitales tienen que estar acreditados para participar en el programa de trasplante renal con donación cruzada. En la actualidad son ya 13 los centros españoles adscritos:
- Hospital Clínic i Provincial de Barcelona.
- Hospital Doce de Octubre de Madrid.
- Hospital Fundació Puigvert de Barcelona.
- Complejo Hospitalario Universitario de A Coruña.
- Hospital Universitario de Bellvitge, de Barcelona.
- Hospital Universitario de La Paz, de Madrid.
- Hospital Virgen de las Nieves de Granada.
- Hospital Virgen del Rocío de Sevilla.
- Germans Trías i Pujol de Badalona
- Hospital Puerta del Mar de Cádiz
- Sant Joan de Deu, de Barcelona
- Hospital Carlos Haya de Málaga
- Hospital la Fe de Valencia
PROGRAMA DE TRASPLANTE RENAL CRUZADO
Según los datos de la ONT, hasta el momento se han inscrito en el programa de donación renal cruzada un total de 62 parejas y realizado 12 evaluaciones en momentos diferentes. De ellas, en la actualidad, una vez efectuado este primer trasplante en cadena, permanecen registradas 39. La puesta en marcha de este programa ha permitido efectuar ya cuatro trasplantes de este tipo: los dos primeros realizados en julio de 2009 y los dos siguientes en febrero de 2011.
El fomento de la donación de vivo es uno de los objetivos prioritarios de la ONT, incluido dentro del Plan Estratégico ‘Donación 40’.
########
LA VÍA INTRAÓSEA.
La vía intraósea es una de las vías de administración de medicamentos más desconocidas por la enfermería. La vía intraósea está enmarcada dentro de la forma parenteral.
Lo que conseguiremos al canalizar una acceso intraóseo es acceder a la cavidad medular del hueso; es preferible elegir huesos largos. Esta cavidad está ocupada por una rica red de capilares sinusoides que drenan a un gran seno venoso central.
Indicaciones:
La vía intraósea responde prácticamente igual que una vía venosa periférica, por lo que esta vía está indicada en pacientes en situación de parada cardiorrespiratoria, politraumatizados, shock, grandes quemados… y en pacientes en los que nos resulte imposible conseguir un acceso venoso con urgencia.
Contraindicaciones:
- Fractura ósea: nunca canalizaremos una vía de este tipo en un hueso fracturado o que tengamos sospecha de que pudiera estarlo.
- Infección en el área de inserción del catéter.
- Tejido adiposo excesivo: siempre que sea imposible encontrar referencias anatómicas adecuadas (habitual en pacientes con obesidad mórbida).
- Osteoporosis: por la reducción de la densidad ósea que conlleva.
- Intentos previos de canalización de acceso intraóseo en ese mismo hueso (en las 24h anteriores).
- Procedimientos ortopédicos importantes en la estructura ósea elegida (prótesis).
- Osteopetrosis: conocida también como “enfermedad de los huesos de mármol”.
Riesgos:
- Osteomielitis: pudiéndose deber la infección a una mala asepsia durante la técnica, a un mal cuidado del catéter y del equipo de infusión, etc.
- Extravasación: no es muy habitual.
Zonas de punción:
- En niños menores de 6 años se recomienda pinchar en el extremo proximal de la tibia en su cara interna anterior.
- En niños mayores de 6 años y adultos, en la tibia distal en su cara interna.
Cuidados del catéter:
Los cuidados de enfermería no difieren demasiado de los cuidados de otro tipo de vías:
- Registrar en la historia del paciente la fecha y la hora de inserción, tipo de catéter, lugar de inserción y medicación administrada.
- Mantener una adecuada inmovilización del miembro donde tenemos insertada la vía.
- Comprobar presencia de pulsos distales y aspecto del miembro (color, temperatura…).
- No debemos de colocar un apósito oclusivo.
- Para evitar la aparición de las complicaciones descritas no debemos de mantener el catéter canalizado más de 24h. Lo retiraremos girando suavemente en sentido horario mientras aplicamos tracción en el catéter.
########
OBESIDAD
La obesidad es la acumulación excesiva de grasa corporal, especialmente en el tejido, y que se puede percibir por el aumento del peso corporal cuando supera más de 20% del peso ideal .
El índice de masa corporal (IMC), peso en kilogramos dividido por el cuadrado de la talla en metros (kg/m2), es una indicación simple de la relación entre el peso y la talla que se utiliza frecuentemente para identificar el sobrepeso y la obesidad. La OMS define el sobrepeso como un IMC igual o superior a 25 y la obesidad como un IMC igual o superior a 30.
- Sobrepeso y obesidad en la infancia:
La obesidad infantil es una enfermedad emergente , desde los años noventa hasta hoy tanto en Estados Unidos como en Europa se ha duplicado. España es el cuarto país de la unión europea con mayor número de niños con problemas de sobrepeso y obesidad.
- Causas de la obesidad infantil:
Los principales desencadenantes son los cambios alimentarios y las nuevas formas de vida. Según los expertos lo ideal es que un niño consuma unas dos mil calorías diarias y que, la mitad de ellas sean hidratos de carbono, un tercio grasas y el resto proteínas. En lugar de esto los niños se alimentan cada día peor.
Además del consumo de alimentos con alto contenido en grasas y azúcares, el sedentarismo de muchos niños los hace cada día más obesos. El practicar una actividad física es esencial para su crecimiento y su salud.
Existen además otros factores que determinan la obesidad infantil. Puede haber influencias sociales, fisiológicas, metabólicas y genéticas.
- Consecuencias:
Los malos hábitos adquiridos durante la infancia pueden llevar al niño a sufrir consecuencias negativas para su salud. Algunas de ellas son las siguientes:
. Problemas con los huesos y articulaciones.
. Dificultades para desarrollar algún deporte u otro ejercicio físico debido a la dificultad para respirar y al cansancio.
. Alteraciones del sueño.
Madurez prematura. Las niñas obesas pueden entrar antes en la pubertad, tener ciclos menstruales irregulares, etc…
. Hipertensión, colesterol y enfermedades cardiovasculares en general.
. Problemas hepáticos.
. Desánimo, cansancio, depresión, decaimiento.
. Baja autoestima, aislamiento social, discriminación…
. Trastornos que deriven en bulimia y anorexia nerviosa.
. Problemas cutáneos.
. Diabetes.
- Tratamiento:
El tratamiento de la obesidad infantil no es una tarea fácil, ni para los médicos, ni para la familia ni para los niños ya que hoy en día el tratamiento se basa en la modificación de los estilos de vida, lo que implica la alteración de sus hábitos alimentarios y físicos. Cuanto mayor sea el niño, más difícil será practicar esos cambios, pero no imposible.
El método usado para tratar la obesidad infantil es la combinación de dieta con el aumento de la actividad física, la educación nutricional y el cambio de conductas. Todo esto solo será efectivo si el niño cuenta con el apoyo y estímulo de su familia.
